Kältemittel
Das 1 x 1 der Kältetechnik (Teil 8)
Durch die neue F-Gase-Verordnung sind Kältemitteleigenschaften und -wahl wieder stark in den Fokus gerückt. Diese Verordnung sieht den Ausstieg aus der Verwendung von Kältemitteln mit zu hohem GWP (global warming potential = Treibhauseffekt) vor. Um die Grenzwerte den richtigen Kältemittel zuordnen und gleichzeitig eine professionelle Alternative für die Zukunft finden zu können, ist das folgende Kältemittelwissen von entscheidendem Vorteil. Die Serie „Das 1 x 1 der Kältetechnik“ basiert auf den kostenfreien eLearning-Modulen von Danfoss, die für das interaktive Selbststudium mittels PC konzipiert sind. Die eLearning-Module bieten jeder Zielgruppe, vom Anfänger bis zum Kälteexperten, ein adäquates Angebot (www.learning.danfoss.de).
Definition
Nach DIN EN 378-1 Abs. 3.7.1 ist Kältemittel definiert als „Fluid, das zur Wärmeübertragung in einer Kälteanlage eingesetzt wird, und das bei niedriger Temperatur und niedrigem Druck Wärme aufnimmt und bei höherer Temperatur und höherem Druck Wärme abgibt, wobei üblicherweise Zustandsänderungen des Fluids erfolgen“. Als Zustandsänderung im Sinne der Norm ist eine Änderung des Aggregatzustands gemeint. Das bedeutet, dass im Verdampfer das Kältemittel bei Trockenexpansion üblicherweise vom flüssigen in den gasförmigen und bei unterkritischen Anlagen im Verflüssiger vom gasförmigen in den flüssigen Zustand überführt wird. Kältemittel ist damit dann nötig, wenn das Temperaturniveau für die Abgabe der Wärme angehoben wird. Ist eine Anhebung der Temperatur nicht notwendig, kann auch ein Kälteträger verwendet werden. Kältemittel werden mit dem Buchstaben „R“ für „refrigerant“ (englisch für Kältemittel) bezeichnet. „R“, eine Zahl und ggf. ein Buchstabe spezifizieren das Kältemittel (z.B. R134a).
Halogenkohlenwasserstoffe
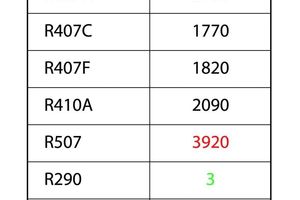
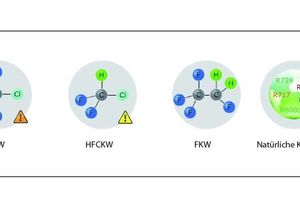
Kältemittel gibt es in den verschiedensten chemischen Varianten. Die heute im gewerblichen Kälteanlagenbau gebräuchlichen Fluorkohlenwasserstoffe (FKW) sind organische Verbindungen. Organische Verbindungen bestehen aus Kohlenstoff- (chemisches Kurzzeichen: C) und Wasserstoffatomen (H). Dabei werden bei FKW Wasserstoffatome durch Fluoratome (F) ersetzt. Diese Kältemittel haben kein Ozonabbaupotential (ODP = ozone depletion potential) – Fluorchlorkohlenwasserstoffe (FCKW) hingegen schon. Vollhalogenierte FCKW sind heute aufgrund des Ozonabbaupotentials verboten. Für diese Eigenschaft ist das Chlor im Molekül verantwortlich. Das waren Kältemittel wie R12 und R502. Bei diesen Kältemitteln waren alle Wasserstoffatome des Kältemittelmoleküls durch Halogene wie Chlor oder Fluor (eventuell auch Brom) ersetzt. Halogene sind Atome der 7. Hauptgruppe des Periodensystems der Elemente. Teilhalogenierte FCKW sind teilweise noch in Benutzung. Das prominenteste Beispiel ist R22. Für Neuanlagen verboten, ist es immer noch für Reparaturen verfügbar. Bei FKW-Kältemitteln ist zwar der Ozonabbau in der Atmosphäre kein Thema, der Treibhauseffekt aber schon. Aus diesem Grund begrenzt die kürzlich verabschiedete europäische F-Gase-Verordnung den Einsatz von R404A und R507 für „normale“ stationäre, gewerbliche Neukälteanlagen auf 2020. Diese beiden Kältemittel sind sehr gebräuchlich und fallen mit ihren GWP von größer als 2500 unter diese Restriktion. GWP-Werte (auf 100 Jahre) divergieren je nach Quelle nicht unerheblich. Letztlich geht es aber für die Praxis nur darum, ob der Wert für das betreffende Kältemittel unterhalb der definierten Grenze liegt.
Weitere Kältemittel
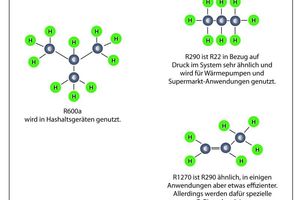
Zusätzlich zu FKW und früher FCKW gibt es noch andere Kältemittel, die verwendet werden. So befindet sich in fast allen Kühlschränken in Mitteleuropa das Kältemittel Isobutan. Isobutan (R600a) ist chemisch gesehen ein reiner Kohlenwasserstoff und in der Summenformel 100 % identisch mit Butan. Rein bedeutet hier, dass im Molekül ausschließlich Kohlen- und Wasserstoffatome vorhanden sind. Isobutan besteht aus vier Kohlenstoffatomen, die aber im Gegensatz zu Butan nicht in Ketten-, sondern in T-Form vorliegen. Isobutan hat keine hohe volumetrische Kälteleistung. Durch sein moderates Druckverhältnis ist es aber dennoch ein sehr energieeffizientes Kältemittel. Ein Nachteil im Gegensatz zu F(C)KW ist die Brennbarkeit von Isobutan. Diese Eigenschaft ist auch bei anderen reinen Kohlenwasserstoffen zu beobachten. So ist Propan (R290) oder Propen (R1270 – Propen ist Propan mit einer Kohlenstoff-Doppelbindung im Molekül) – ebenfalls leicht entflammbar und gleichzeitig ein gutes Kältemittel.
Neben diesen organischen gibt es auch anorganische Verbindungen, die gute Kältemittel abgeben. Ein wichtiges Kältemittel – besonders für Großkälteanlagen – ist Ammoniak (R717). R717 besteht aus einem Stickstoff und drei Wasserstoffatomen. Da hier kein Molekülgerüst aus Kohlenstoffatomen besteht, ist dieses Kältemittel klar als anorganisch zu erkennen. Die volumetrische Kälteleistung und Energieeffizienz sind sehr gut. Allerdings gibt es einen Nachteil. Das Kältemittel ist toxisch und löst auch in geringen Anteilen in der Atemluft bei Menschen Panik aus. Hinsichtlich ODP und GWP ist dieses Kältemittel aber perfekt und wird damit wohl auch in Zukunft die erste Wahl für Großkälteanlagen sein.
Nomenklatur
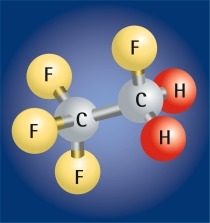
Um festzustellen, was sich genau hinter einer Kältemittelbezeichnung verbirgt, gibt es folgende Möglichkeit. Bei Einstoffkältemitteln kann an der „R“-Bezeichnung die chemische Zusammensetzung abgeleitet werden. Bei den organischen Kältemitteln (ohne 4er-, 5er- und 7er-Reihe) ist die erste Stelle die Anzahl der Kohlenstoffatome minus eins, danach die Anzahl der Wasserstoffatome plus eins und an dritter Stelle die Anzahl der Fluoratome. Somit hat das R134a-Molekül zwei „C“-, zwei „H“- und vier „F“-Atome. Bei Einstoffkältemitteln, wie in unserem Beispiel R134a, kann zusätzlich noch ein kleiner Buchstabe der Typenbezeichnung nachgestellt sein. Dies beschreibt die Isometrie, also die Symmetrie, des Kältemittels. Je symmetrischer das Kältemittel aufgebaut ist, ein umso früherer Buchstabe im Alphabet wird verwendet. D.h., ohne Buchstaben hat das Molekül die größte Symmetrie. Über die Endungen a, b, c wird das Molekül immer einseitiger in der Atom- und Gewichtsverteilung. Sollte das Kältemittel nur zwei Stellen haben, so ist ihm zur Anwendung dieser Regel eine „0“ voranzustellen. Somit ist R22 als R022 zu behandeln und besteht aus einem „C“-, einem „H“- und zwei „F“-Atomen. In diesem Fall fehlt aber noch ein Atom, da Kohlenstoff immer vier Bindungen hat, aber erst drei Atome „angedockt“ sind. Das bedeutet, es wird der Rest mit Chloratomen ergänzt. R22 hat damit ein Chloratom pro Molekül. Damit erklärt sich auch das Ozonabbaupotential von R22 von 0,055. Das Referenzkältemittel für das ODP ist das verbotene R12 mit dem Wert 1. Kältemittel ohne Chlor (und Brom) haben kein Ozonabbaupotential. Sollte das Kältemittel Brom enthalten sein, so wird die Anzahl der enthaltenen Atome einfach der Zahl nachgestellt. Z.B. R13B1 enthält drei Fluor- und ein Bromatom.
Die chemische Formel von Kältemittelgemischen kann nicht mit diesem Schlüssel aufgelöst werden. Mischungen sind allesamt den 4er- und 5er-Gruppen zugeordnet. Prominente Beispiele sind die Kältemittel R404A und R507. Der Buchstabenappendix bei Kältemittelgemischen ist immer ein Groß-, nicht wie bei der Isometrie ein Kleinbuchstabe. Dieser Großbuchstabe legt die Gemischanteile des Kältemittels fest. Somit hat R407F ein anderes Mischungsverhältnis seiner Anteile, aber die gleichen chemischen Stoffe als Bestandteil wie R407C. Kältemittelgemische können aus zwei oder mehr Bestandteilen bestehen. Durch die Kombination aus verschiedenen Stoffen kann ein Kältemittelgemisch einen Gleit aufweisen. Das bedeutet, dass sich die Temperatur während des Aggregatszustandsübergangs ändert. Bei den zeotropen Kältemittelgemischen der 4er-Reihe, besonders bei R407A, C und F ist dieser Gleit deutlich ausgeprägt, bei azeotropen Gemischen nicht (5er-Reihe). Sie verhalten sich nahezu wie Einstoffkältemittel. Bei Einstoffkältemitteln gibt es je nach Druck immer nur einen Siedepunkt und somit keinen Gleit.
Für die natürlichen Kältemittel, vorzugsweise anorganische Verbindungen, gibt es die 7er-Gruppe. In dieser sind bekannte Beispiele R744/CO2 und R717/NH3 bzw. Ammoniak. Die chemische Summenformel lässt sich auch hier ableiten, allerdings mit einer anderen Methode als bei den organischen Stoffen. Die Zahl hinter der „7“ ist die Molekülmasse des natürlichen Kältemittels. So summieren sich bei CO2 das Kohlenstoffatom zu 12 und die beiden Sauerstoffatome (O) zu je 16 zu letztendlich 44 (siehe Periodensystem der Elemente). Bei R717 sind es 14 für Stickstoff (N) und drei Wasserstoff mit je 1. R723 fällt nicht unter diese Regel.
Ersatz für R404A und R507
Für Kälteanlagenbauer ist besonders das Verbot von R404A und R507 in stationären Neuanlagen zum Jahr 2020 eine große Herausforderung. Als bereits gebräuchliche Alternativen stehen R134a und R407C zur Verfügung. Zwei weitere Kältemittel sind R407A und R407F. Für Normalkühlung und Klima können alle diese Kältemittel problemlos verwendet werden. Ein kleiner Nachteil stellt der Gleit von R407A, C und F dar. Für viele Kälteanlagenbauer ist dieser Effekt aber nicht fremd, da R407C zu den am meisten verbreiteten Kältemittel gehört. Bezüglich des Treibhauseffekts und der Energieeffizienz ist besonders R134a unter den benannten Alternativen die beste Wahl. Nachteile sind die höheren Investitionskosten bei Neuanlagen aufgrund des größeren Volumenstroms verglichen mit den benannten 4er-Kältemitteln. Außerdem ist R134a mit einer Nassdampftemperatur von -26 °C bei Umgebungsdruck nur bedingt für Tiefkühlung geeignet, da die Verdampfungstemperatur dann unterhalb des Luftdrucks liegen würde. Das ist zwar möglich, im Falle einer Undichte wird aber Umgebungsluft auf der Saugseite in die Anlage gezogen. Bei den Kältemitteln der 4er-Reihe liegt die Problematik eher in der hohen Druckgasendtemperatur im Tiefkühleinsatz. Eine Alternative mit besonders niedrigem Treibhauspotential ist R290 (Propan). Abgesehen von der Brennbarkeit ähnelt dieses Kältemittel in der Anwendung sehr stark R22. Druck/Temperatur, Öl und Kälteleistung sind sehr ähnlich. Allein die Brennbarkeit erfordert ggf. zusätzliche Maßnahmen. R717 hat eine sehr gute volumetrische Kälteleistung und ist umwelttechnisch über jeden Zweifel erhaben. Daher ist zu erwarten, dass sich dieses Großkälte-Kältemittel weiter behauptet und auch in niedrigere Leistungsregionen als bisher vorstoßen wird. „Last but not least“ ist da noch R744 (CO2). Dieses Kältemittel wird immer mehr verwendet und ist mit ODP 0 und GWP 1 ein Glücksfall für die Umwelt. Die Anwendung in Kaskadenkälteanlagen für die Tiefkühlung und mit z.B. R134a oder R290 in der oberen Stufe hat sich bereits bestens bewährt. Ob die alleinige Anwendung von CO2 in transkritischen Kälteanlagen ihren Siegeszug auch in südlichere Gefilde fortsetzen wird, bleibt abzuwarten.